في عالم الكيمياء العضوية، حيث تتعدد التفاعلات وتتشابك آلياتها، لا تحدث التحولات الكيميائية بصورة عشوائية، بل تحكمها قواعد علمية دقيقة تمكّن الكيميائيين من التنبؤ بمسارات التفاعل ونواتجه بدرجة عالية من الدقة.
كتب المهندس أمجد قاسم
X@amjad
من بين أبرز القواعد التي تحكم التفاعلات العضوية قانون ماركوفنكوف (Markovnikov’s Rule) بوصفه أحد أهم المبادئ التي تفسر اتجاه تفاعلات الإضافة على المركبات غير المشبعة مثل الألكينات والألكاينات، خاصة في تفاعلات إضافة هاليدات الهيدروجين أو الماء.
وقد شكّل هذا القانون، رغم بساطة صياغته، نقلة نوعية في فهم كيفية توزيع الذرات أثناء التفاعل، وتفسير سبب تكوّن ناتج رئيسي دون غيره اعتمادًا على استقرار النواتج الوسيطة مثل الكربوكاتيونات.
في هذا المقال نسلط الضوء على هذا القانون المحوري، ونتعرف على العالم الذي وضع أسسه، ونستعرض أهم تطبيقاته مع أمثلة ومعادلات كيميائية توضح دوره في تفسير آليات تفاعلات الإضافة وأهميته المستمرة في دراسة وتطبيقات الكيمياء العضوية الحديثة.
من هو ماركوفنكوف؟
فلاديمير فاسيليفيتش ماركوفنكوف (Vladimir Markovnikov) هو كيميائي روسي وُلد عام 1837، وقد اشتهر بإسهاماته في الكيمياء العضوية، خاصة في دراسة تفاعلات الإضافة على الهيدروكربونات غير المشبعة.
وفي عام 1869 اقترح القاعدة التي حملت اسمه، والتي تفسر اتجاه إضافة المتفاعلات إلى الروابط الثنائية في الألكينات. (Chemistry LibreTexts)
وقد ساهم هذا القانون في تطوير فهم آليات التفاعل وخاصة فكرة استقرار الكربوكاتيونات (Carbocations)، وهو مفهوم أساسي في تفسير الكثير من تفاعلات الكيمياء العضوية الحديثة.
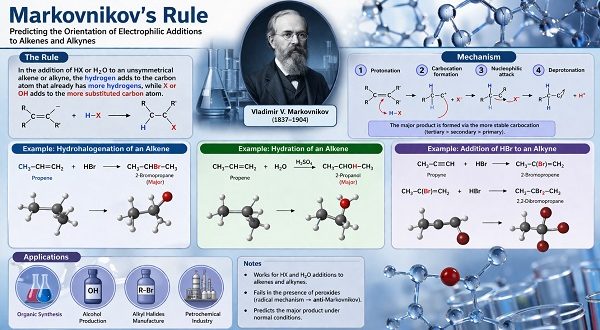
ما هو قانون ماركوفنكوف؟
ينص قانون ماركوفنكوف على أنه:
عند إضافة حمض هاليدي (HX) إلى ألكين غير متماثل، فإن ذرة الهيدروجين ترتبط بذرة الكربون التي تحتوي على عدد أكبر من ذرات الهيدروجين، بينما ترتبط ذرة الهالوجين بذرة الكربون الأكثر استبدالاً بالمجموعات الألكيلية. (Chemistry Steps)
بصيغة أبسط:
- الهيدروجين يذهب إلى الكربون “الأغنى بالهيدروجين”.
- الهالوجين يذهب إلى الكربون “الأغنى بالمجموعات الكربونية”.
والسبب في ذلك هو تكوّن أيون كربوني أكثر استقراراً أثناء التفاعل.
تطبيق قانون ماركوفنكوف في إضافة هاليد الهيدروجين إلى الألكينات
تسمى هذه التفاعلات بتفاعلات الهيدروهالوجنة (Hydrohalogenation)، حيث يتم إضافة HX مثل HCl أو HBr أو HI إلى الرابطة الثنائية.
مثال كيميائي:
إضافة HBr إلى البروبين:
CH₃–CH=CH₂ + HBr → CH₃–CHBr–CH₃
في هذا التفاعل:
- يضاف الهيدروجين إلى الكربون الطرفي (CH₂)
- يضاف البروم إلى الكربون الأوسط
آلية التفاعل:
يمر التفاعل بخطوتين رئيسيتين:
- إضافة البروتون (H⁺) وتكوين كربوكاتيون:
CH₃–CH=CH₂ + H⁺ → CH₃–C⁺H–CH₃
- هجوم أيون الهاليد:
CH₃–C⁺H–CH₃ + Br⁻ → CH₃–CHBr–CH₃
والسبب في تكوّن هذا الناتج هو أن الأيون الكربوني الثانوي أكثر استقراراً من الأيون الكربوني الأولي. (Master Organic Chemistry)
تطبيق قانون ماركوفنكوف في إضافة الماء إلى الألكينات (تفاعل الإماهة)
يمكن أيضاً تطبيق القانون في تفاعل إضافة الماء (Hydration) بوجود حمض قوي مثل H₂SO₄ كعامل حفاز.
مثال:
إضافة الماء إلى البروبين بوجود حامض الكبريتيك كعامل مساعد:
CH₃–CH=CH₂ + H₂O → CH₃–CHOH–CH₃
الناتج هو 2-بروبانول وليس 1-بروبانول، وذلك حسب قانون ماركوفنكوف.
تطبيق القانون على الألكاينات
ينطبق قانون ماركوفنكوف أيضاً على الألكاينات عند إضافة HX أو الماء، ولكن التفاعل يكون أبطأ بسبب انخفاض استقرار الكربوكاتيون الفينايلي مقارنة بالألكانات. (Chempedia)
مثال:
إضافة HBr إلى البروباين:
CH₃–C≡CH + HBr → CH₃–C(Br)=CH₂
وعند إضافة جزيء ثانٍ:
CH₃–C(Br)=CH₂ + HBr → CH₃–CBr₂–CH₃
أهمية قانون ماركوفنكوف في الكيمياء العضوية
تكمن أهمية هذا القانون في عدة نقاط:
- التنبؤ بنواتج التفاعل
يساعد الكيميائيين على معرفة الناتج الرئيسي دون الحاجة إلى التجربة.
- فهم آليات التفاعل
يرتبط القانون بمفهوم استقرار الأيون الكربوني، وهو أساس تفسير الكثير من التفاعلات.
- التطبيقات الصناعية
يستخدم في:
- تصنيع الكحولات
- إنتاج الهاليدات الألكيلية
- الصناعات البتروكيميائية
- تصميم التخليق العضوي
يساعد في اختيار المسارات المناسبة لتحضير المركبات العضوية المعقدة.
ملاحظات مهمة حول قانون ماركوفنكوف
رغم أهميته، توجد حالات لا ينطبق فيها القانون مثل:
- وجود فوق الأكاسيد (Peroxides)
- تفاعلات الجذور الحرة
- تفاعلات Anti-Markovnikov
خاتمة
يعد قانون ماركوفنكوف من أهم القواعد التفسيرية في الكيمياء العضوية، إذ يوفر وسيلة بسيطة لكنها قوية للتنبؤ باتجاه تفاعلات الإضافة.
وقد أثبت هذا القانون، منذ القرن التاسع عشر وحتى اليوم، قيمته العلمية والعملية في فهم سلوك المركبات غير المشبعة وتطوير الصناعات الكيميائية.
ولا يزال هذا القانون من الأدوات الأساسية التي يعتمد عليها طلاب الكيمياء والباحثون، خاصة في مجالات التخليق العضوي والكيمياء الصناعية.
المراجع
- Chemistry LibreTexts – Markovnikov’s Rule
Markovnikov’s Rule explanation - Master Organic Chemistry – Hydrohalogenation of Alkenes
Hydrohalogenation and Markovnikov rule - Chemistry Steps – Markovnikov’s Rule
Detailed explanation of Markovnikov’s rule
 آفاق علمية وتربوية موقع متخصص بالثقافة العلمية والتربوية
آفاق علمية وتربوية موقع متخصص بالثقافة العلمية والتربوية

مع جزيل الشكر على هذا المقال العلمي المميز